Das angeborene Immunsystem und seine zahlreichen Bestandteile – Teil 1: Barrieren und Zelltypen
Inhaltsverzeichnis
Unser Immunsystem ist ein hochkomplexes, fein abgestimmtes Netzwerk aus Zellen, Molekülen und Geweben, das uns vor schädlichen Eindringlingen wie Bakterien, Viren, Pilzen und Parasiten schützt. Dabei lässt es sich in zwei große funktionelle Einheiten unterteilen: das angeborene (unspezifische) und das adaptive (spezifische) Immunsystem. Beide Systeme arbeiten eng zusammen, unterscheiden sich jedoch in ihrer Wirkungsweise, Reaktionsgeschwindigkeit und Spezifität.
In diesem Artikel erfährst du viele wichtigen Informationen zu den verschiedenen Barrieren des angeborenen Immunsystems und welche Aufgaben die verschiedenen Immunzellen bei dieser Immunantwort haben.

Christina Winzig ist Wissenschaftlerin aus Überzeugung – mit einer besonderen Leidenschaft dafür, komplexe Zusammenhänge einfach und greifbar zu machen. Schon während ihres Studiums arbeitete sie in Australien an spannenden Forschungsprojekten, bei denen die Wirkstoffe aus Spinnen-, Skorpion- und Schneckengiften auf ihre mögliche Anti-Krebs-Wirkung untersucht wurden. Diese Arbeit weckte ihre Begeisterung für die Möglichkeiten der Wissenschaft und den Wunsch, Erkenntnisse sinnvoll in die Praxis zu übertragen.
Mit ihrer Weiterbildung zur Medizinredakteurin verlagerte sich ihr Fokus auf die ganzheitliche Gesundheit. Durch zahlreiche Fortbildungen in Labormedizin, präventiver Medizin, Immunologie, Nährstoffkunde und ganzheitlichen Therapien baute sie ihre Expertise weiter aus. Besonders am Herzen liegt ihr die Arbeit mit Laborwerten: Für Christina sind sie ein unschätzbares Werkzeug, um sowohl in der Prävention als auch bei der Suche nach den Ursachen von Beschwerden Klarheit zu schaffen und gezielt vorzugehen.
Heute widmet sie sich der Aufgabe, Menschen dabei zu helfen, ihre Gesundheit besser zu verstehen und aktiv zu gestalten. Ihr Ziel ist es, medizinisches Wissen so aufzubereiten, dass es für jeden zugänglich und anwendbar wird – immer mit dem Blick auf die gesamte Person und die bestmögliche Unterstützung für ein gesundes Leben.
Du erreichst Christina über ihre Homepage https://molekularmedizinerin.de/ und über Instagram.
Bedeutung des angeborenen Immunsystems
Das angeborene Immunsystem stellt die erste Verteidigungslinie gegen pathogene Mikroorganismen dar. Es reagiert schnell und unspezifisch auf eine Vielzahl potenziell gefährlicher Erreger. Ziel ist es, das Eindringen und die Ausbreitung von Krankheitserregern frühzeitig zu verhindern oder einzudämmen und das idealerweise noch bevor eine spezifische Immunantwort notwendig wird.
Diese schnelle Reaktion ist besonders in den ersten Stunden bis Tagen einer Infektion von zentraler Bedeutung. Zudem spielt das angeborene Immunsystem eine entscheidende Rolle bei der Aktivierung und Modulation der adaptiven Immunantwort, indem es dem Körper hilft, spezifische Abwehrmechanismen gezielt und effektiv einzuleiten.
Darüber hinaus ist das angeborene Immunsystem auch an der Aufrechterhaltung der Gewebehomöostase beteiligt, erkennt und eliminiert geschädigte oder entartete Zellen und unterstützt die Wundheilung durch Freisetzung regenerativer Signalmoleküle.
Abgrenzung zum adaptiven Immunsystem
Im Gegensatz zum angeborenen Immunsystem ist das adaptive Immunsystem hochspezifisch und lernt durch Erfahrung (Abbildung 1). Es entwickelt gezielte Immunantworten gegen individuell erkannte Antigene und bildet ein immunologisches Gedächtnis, das bei wiederholtem Kontakt mit demselben Erreger zu einer schnelleren und effektiveren Reaktion führt.
Während das angeborene System innerhalb von Minuten bis wenigen Stunden aktiv wird, braucht das adaptive Immunsystem mehrere Tage zur Entwicklung einer maßgeschneiderten Abwehr. Zu den zentralen Akteuren des adaptiven Systems zählen B-Zellen, T-Zellen und die von ihnen gebildeten Antikörper.
Trotz dieser Unterschiede sind beide Systeme eng miteinander verflochten. Ohne die „Vorarbeit“ des angeborenen Immunsystems kann das adaptive Immunsystem nicht effizient aktiviert werden. Umgekehrt beeinflusst das adaptive System durch Rückkopplungsschleifen die Aktivität und Regulation der angeborenen Immunantwort.
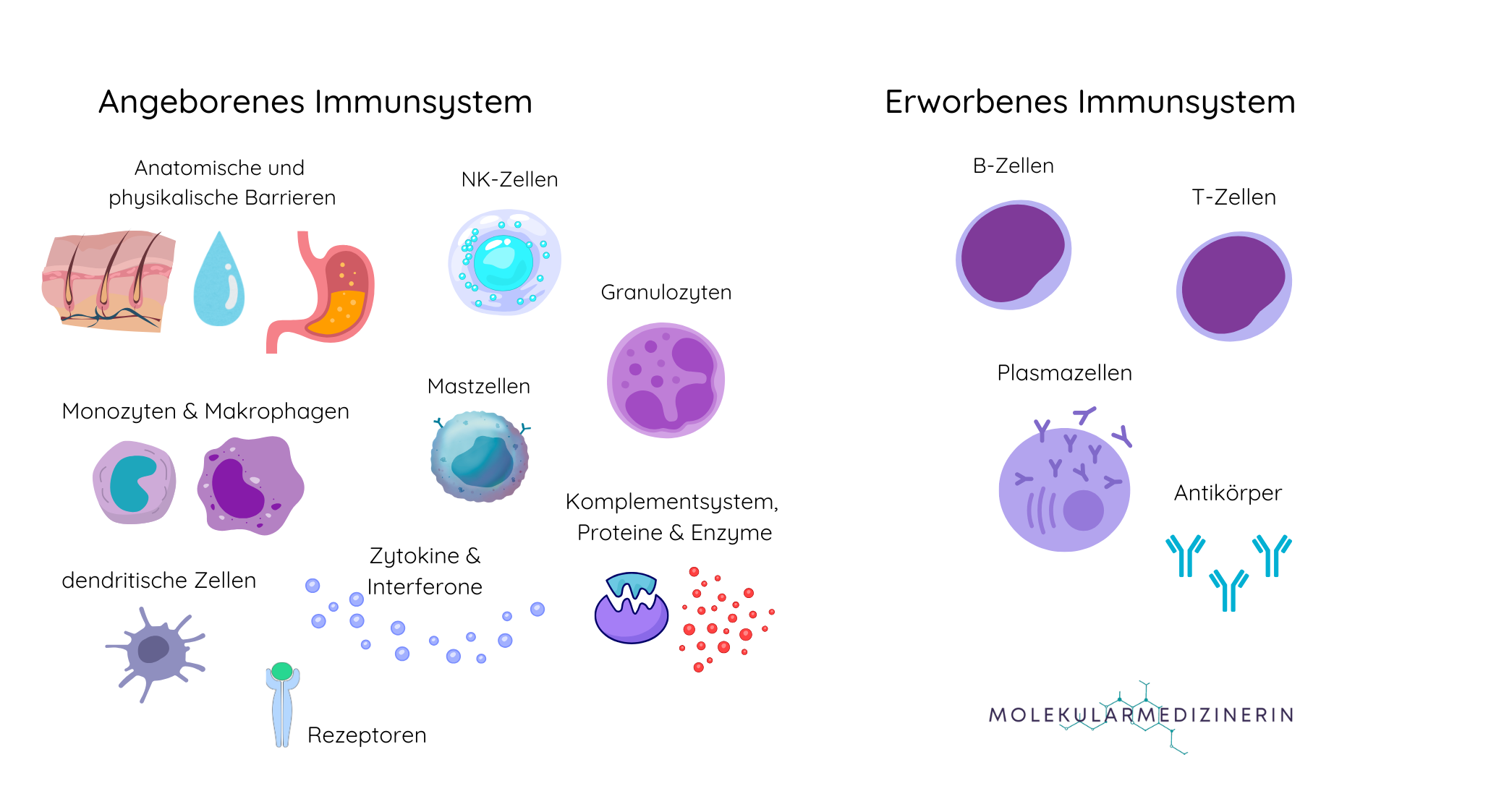
Abbildung 1 Das angeborene Immunsystem kann bereits innerhalb weniger Minuten aktiv werden. Die erworbene Immunantwort hingegen lernt aus den Informationen der angeborenen Immunantwort, was längere Zeit in Anspruch nimmt.
Überblick über die Hauptkomponenten des angeborenen Immunsystems
Das angeborene Immunsystem umfasst eine Vielzahl unterschiedlicher physikalischer, chemischer und zellulärer Abwehrmechanismen. Dazu gehören:
- Physikalische Barrieren wie Haut und Schleimhäute, die das Eindringen von Krankheitserregern verhindern.
- Chemische Barrieren wie antimikrobielle Peptide, Enzyme und saure Umgebungen, die Mikroorganismen direkt schädigen oder deren Wachstum hemmen.
- Zelluläre Komponenten, darunter Phagozyten (z. B. Makrophagen und neutrophile Granulozyten), natürliche Killerzellen (NK-Zellen) und dendritische Zellen, die Erreger erkennen, zerstören und die Immunantwort koordinieren.
- Das Komplementsystem, ein Netzwerk aus im Blut zirkulierenden Plasmaproteinen, das Pathogene markiert, Zellzerstörung auslöst und Entzündungsprozesse fördert.
- Mediatoren wie Zytokine, Chemokine und Akute-Phase-Proteine, die als Botenstoffe die Kommunikation zwischen Immunzellen ermöglichen und Entzündungsprozesse steuern.
Im Zusammenspiel bildet dieses komplexe Netzwerk einen äußerst effektiven Schutzmechanismus, der nicht nur gegen pathogene Mikroorganismen wirkt, sondern auch auf Gewebeschäden, Fremdkörper und Veränderungen im inneren Milieu reagiert.
Die Barrieren
Physikalische Barrieren
Die physikalischen Barrieren des Körpers bilden die erste Schutzschicht gegen Krankheitserreger und Fremdstoffe – sie wirken rein mechanisch und verhindern, dass Mikroorganismen überhaupt in den Körper eindringen können. Eine zentrale Rolle spielt dabei die Haut, die als größte Barrierefläche mit ihrer Hornschicht aus abgestorbenen, verhornten Zellen einen robusten Schutzschild bildet (Abbildung 2). Sie ist in eine Lipidmatrix (also in Fettsäuren) eingebettet und wird durch einen leicht sauren pH-Wert der Talg- und Schweißdrüsen unterstützt, was effektiv das Wachstum von Keimen hemmt. Zusätzlich produzieren Hautzellen antimikrobielle Peptide wie Defensine, die aktiv gegen pathogene Mikroben wirken.
Auch die Schleimhäute des Atem-, Verdauungs- und Urogenitaltrakts leisten einen wichtigen Beitrag zur Immunabwehr. Sie sind mit schützendem Schleim überzogen, der Mikroorganismen bindet und deren Eindringen erschwert. Besonders in den Atemwegen sorgt die sogenannte mukoziliäre Clearance dafür, dass Schleim mitsamt Erregern durch koordinierte Bewegung feiner Flimmerhärchen in Richtung Rachen transportiert wird. Dort kann der Schleim dann abgehustet oder verschluckt werden.
Ein weiterer wichtiger Schutzmechanismus sind die sogenannten Tight Junctions im Darm. Das sind enge Zellverbindungen zwischen Epithelzellen, die den Durchtritt von Keimen, Toxinen und Allergenen zwischen den Zellen verhindern. Wird diese Barriere durch Entzündungen, Umweltfaktoren oder bestimmte Nahrungsbestandteile gestört, kann es zu erhöhter Durchlässigkeit kommen, was das Risiko für chronisch-entzündliche Erkrankungen erhöhen kann. Dies ist auch bekannt als „Leaky Gut“ oder gestörte Schleimhautbarriere.
Ergänzt werden diese Barrieren durch weitere mechanische Schutzmaßnahmen wie den kontinuierlichen Fluss von Tränen, Speichel und Urin, die Mikroorganismen ausspülen, sowie durch Reflexe wie Husten und Niesen, die Erreger aus den Atemwegen entfernen. Auch die Peristaltik des Darms trägt zur raschen Weiterbeförderung potenziell schädlicher Substanzen bei, ebenso wie der zervikale Schleimpfropf, der den Gebärmutterhals zeitweise abdichtet und so das Eindringen von Keimen verhindert.
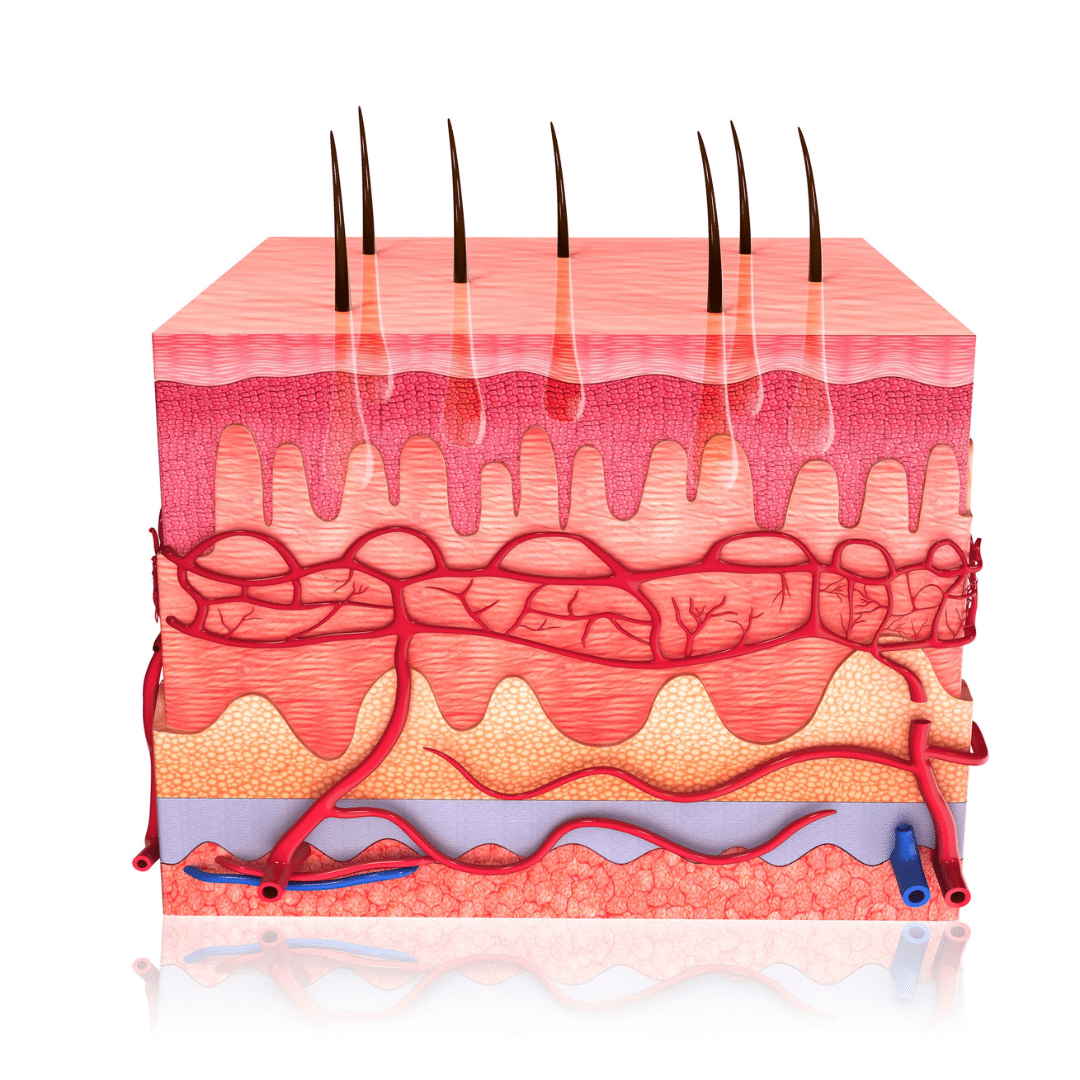
Abbildung 2 Das Immunsystem schützt uns mit seinen physikalischen Barrieren, wie Haut und Schleimhäute, vor Krankheitserregern.
Chemische Barrieren
Neben den mechanischen Schutzsystemen bilden chemische Barrieren eine essenzielle Säule des angeborenen Immunsystems. Sie wirken durch antimikrobielle Moleküle, Enzyme und saure Milieus, die Mikroorganismen aktiv hemmen oder zerstören. Diese Schutzmechanismen sind an sämtlichen Grenzflächen des Körpers aktiv, wie etwa auf Haut, Schleimhäuten, in Speichel, Tränen, Magensaft oder Vaginalsekret.
Eine zentrale Rolle spielen antimikrobielle Peptide (AMPs) wie Defensine und Cathelicidine. Diese werden von Epithelzellen und Immunzellen gebildet und zerstören gezielt die Zellmembranen von Bakterien, Viren und Pilzen. Besonders an Haut und Schleimhäuten sind sie wichtige Schutzfaktoren im Alltag.
Auch enzymatische Substanzen tragen zur chemischen Abwehr bei:
Lysozym
– Enthalten in Tränen, Speichel und Schleim
– Zerstört bakterielle Zellwände
Lactoferrin
– Bindet Eisen und entzieht es pathogenen Keimen
Peroxidasen
– Erzeugen reaktive Sauerstoffverbindungen, die Mikroorganismen schädigen
Sekretorisches IgA
– wirkt ebenfalls frühzeitig an den Schleimhautoberflächen, indem es Erreger neutralisiert und ihre Anhaftung verhindert (obwohl Teil der adaptiven Immunantwort)
Besonders effektiv ist die Magensäure mit einem extrem niedrigen pH-Wert von 1–2. Sie zerstört die meisten Keime, bevor sie in den Darm gelangen (Abbildung 3). Auch im weiteren Verdauungstrakt wirken Verdauungsenzyme und Gallensäuren antimikrobiell. Darüber hinaus nutzen auch andere Körperregionen den pH-Wert als Waffe: Die Haut sowie der Vaginalbereich sind gezielt sauer, um krankmachende Keime in Schach zu halten.
Nicht zuletzt wirken viele Körperflüssigkeiten doppelt: Sie spülen Erreger nicht nur mechanisch aus dem Körper, sondern enthalten gleichzeitig antimikrobielle Substanzen. Beispiele sind Tränen, Speichel, Bronchial- oder Vaginalsekrete. Sie alle verbinden physikalischen Schutz mit chemischer Abwehr auf elegante Weise.
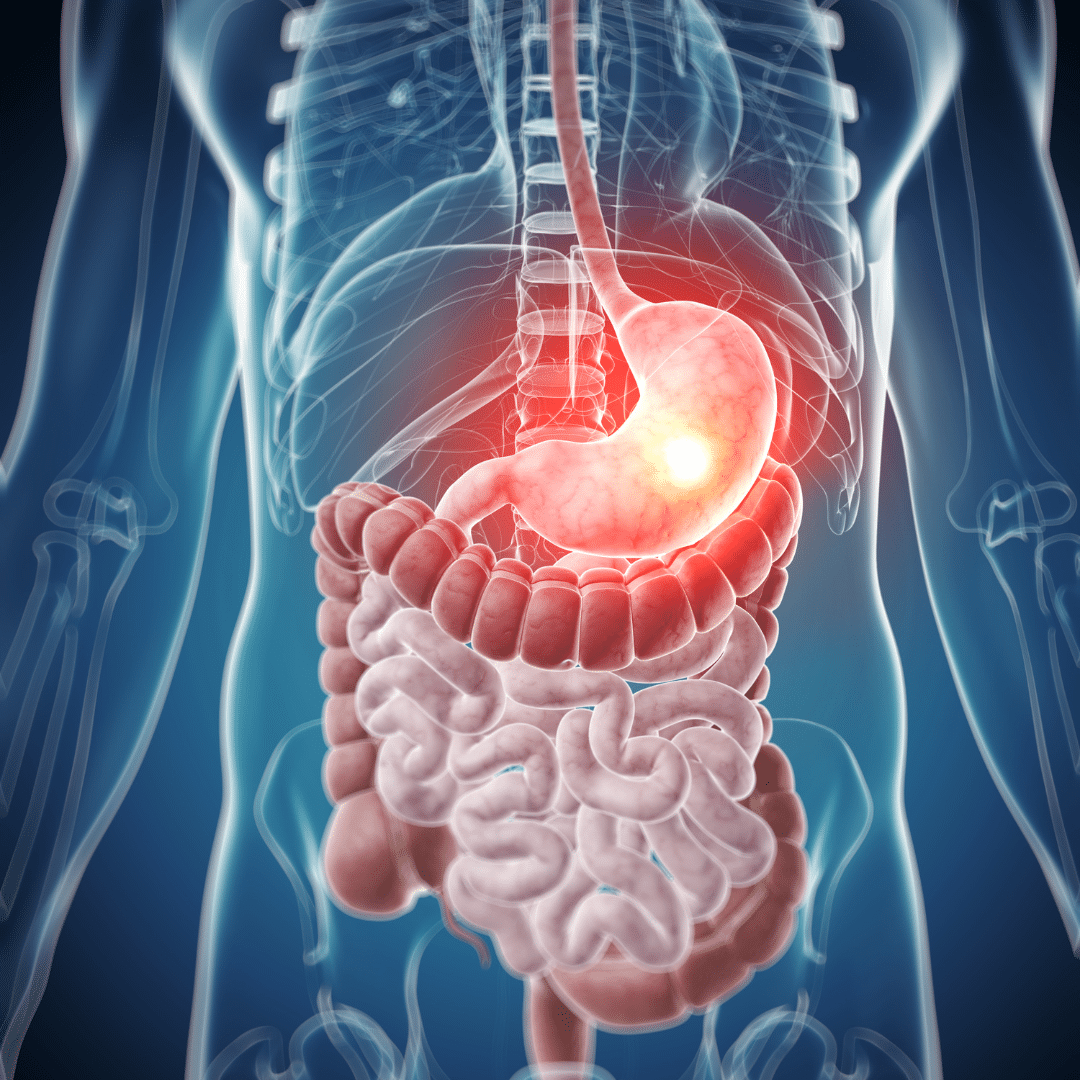
Abbildung 3 Die Magensäure ist nicht nur für die Verdauung wichtig, sondern auch ein sehr wichtiger Bestandteil in der Abwehr von Krankheitserregern.
Zelluläre Komponenten des angeborenen Immunsystems
Die zellulären Bestandteile des angeborenen Immunsystems sind hochaktive Immunzellen, die eindringende Erreger erkennen, bekämpfen und gleichzeitig die Kommunikation mit anderen Immunzellen koordinieren. Im Gegensatz zum adaptiven Immunsystem benötigen sie keine vorherige Sensibilisierung, sondern reagieren sofort auf universelle molekulare Muster, sogenannte Pathogen-assoziierte molekulare Muster (PAMPs) oder Schaden-assoziierte molekulare Muster (DAMPs). Erkannt werden diese Muster über Mustererkennungsrezeptoren (PRRs) wie Toll-like-Rezeptoren (TLRs).
PAMPs
PAMPs (Pathogen-associated molecular patterns; dt. Pathogen-assoziierte molekulare Muster) sind molekulare Strukturen auf Mikroorganismen wie Bakterien, Viren und Pilzen, die vom angeborenen Immunsystem des menschlichen Körpers als „fremd“ erkannt werden. Sie dienen dem Immunsystem dazu, eine Infektion zu erkennen und eine Immunantwort auszulösen, indem sie von sogenannten Mustererkennungsrezeptoren (PRRs) erkannt werden. Beispiele für PAMPs sind Lipopolysaccharide (LPS) auf Bakterien oder RNA und DNA von Viren.
DAMPs
DAMPs ist die Abkürzung für Damage-Associated Molecular Patterns (dt. Schaden-assoziierte molekulare Muster) und bezeichnet endogene Moleküle, die von der eigenen Zelle stammen und als Gefahrensignale wirken, wenn eine Gewebeschädigung oder eine Schädigung der Zelle vorliegt (z.B. Hitzeschockproteine). Sie werden von Rezeptoren des Immunsystems erkannt und lösen eine Entzündungsreaktion aus, um den Schaden zu reparieren und eine Immunantwort zu initiieren.
Neutrophile Granulozyten
Neutrophile sind die häufigsten weißen Blutkörperchen und die ersten Zellen, die bei einer Infektion am Ort des Geschehens eintreffen (Abbildung 4). Sie sind besonders effizient in der Phagozytose, dem „Fressen“ und Abbau von Bakterien, Pilzen und Zelltrümmern. Zusätzlich setzen sie reaktive Sauerstoffspezies (ROS) und Enzyme wie Elastase frei, um Erreger zu zerstören.
Eine besondere Funktion ist die Bildung von Neutrophil Extracellular Traps (NETs). Das sind netzartige Strukturen aus DNA und Enzymen, die Mikroorganismen einfangen und neutralisieren.
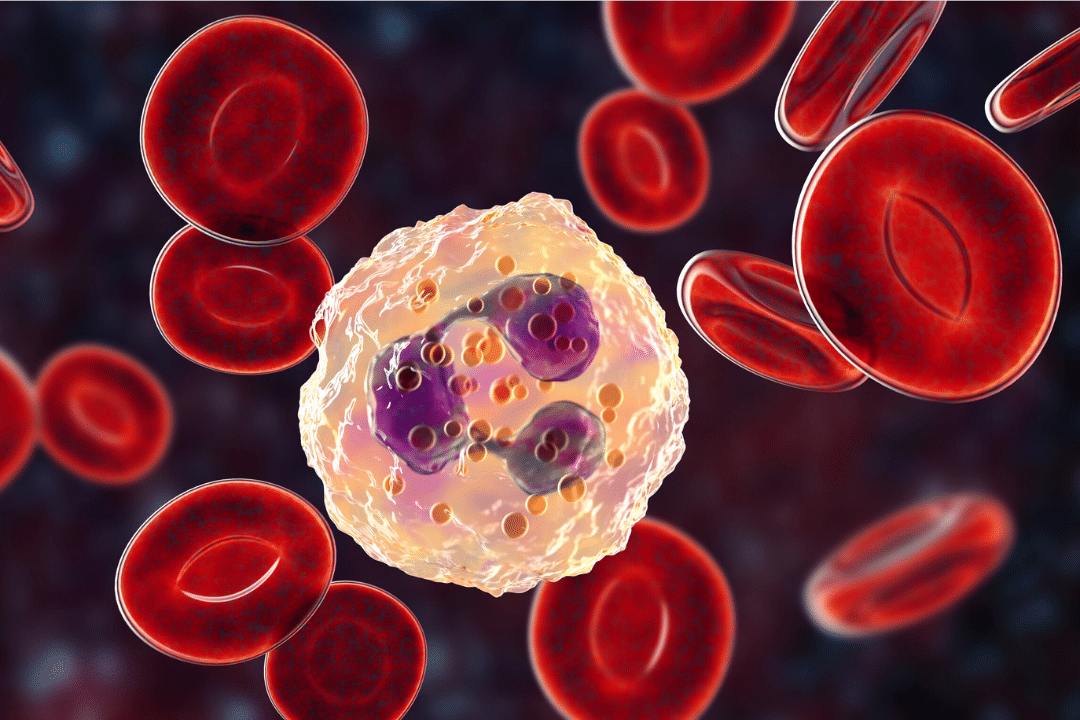
Abbildung 4 Neutrophile Granulozyten sind Teil der angeborenen Immunantwort. Sie können Bakterien, Pilze und Zelltrümmer aufnehmen und beseitigen.
Makrophagen
Makrophagen („große Fresszellen“) entstehen aus Monozyten, die ins Gewebe einwandern und sich dort weiterentwickeln (Abbildung 5). Sie sind wichtige Phagozyten, erkennen Erreger über PRRs (Mustererkennungsrezeptoren) und bauen diese ab. Darüber hinaus produzieren sie entzündungsfördernde Zytokine (z. B. TNF-α, IL-1β, IL-6), die andere Immunzellen anlocken und das Entzündungsgeschehen steuern.
Makrophagen haben auch eine zentrale Rolle in der Gewebehomöostase, da sie beschädigte Zellen und Zelltrümmer entfernen. Sie wirken sowohl pro-entzündlich (M1-Polarisation) als auch entzündungsauflösend und heilungsfördernd (M2-Polarisation). Dies ist jeweils abhängig vom Gewebemilieu.
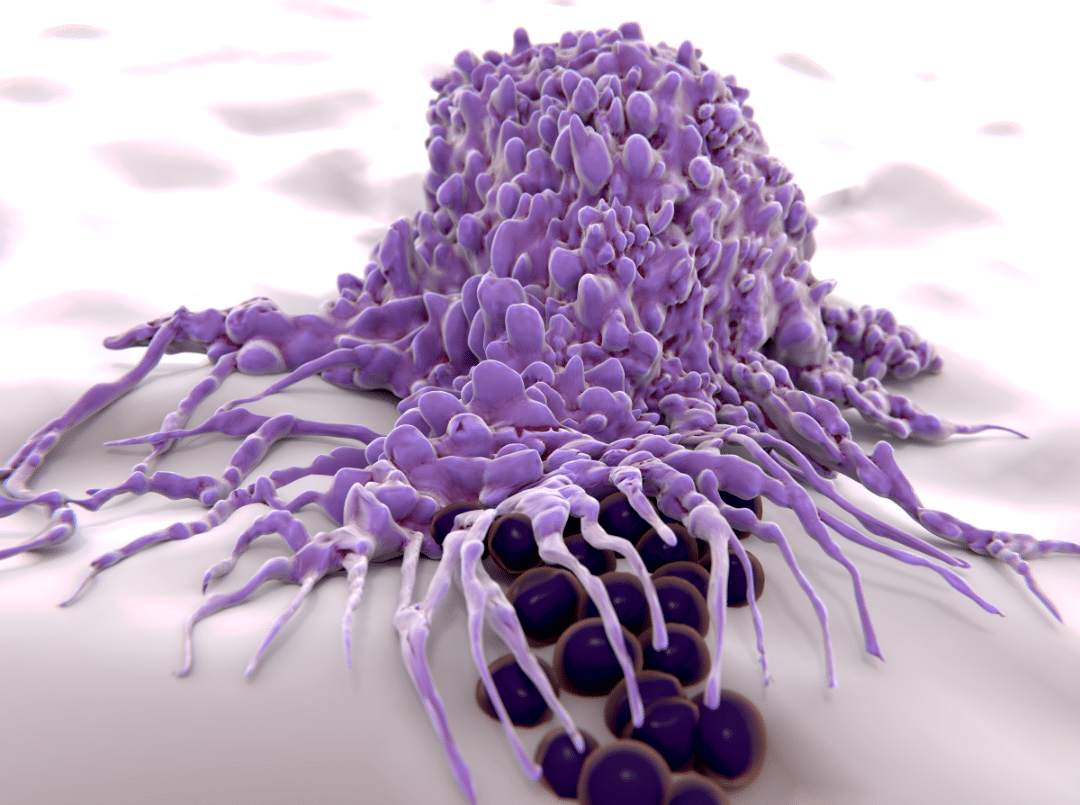
Abbildung 5 Makrophagen, auch große Fresszellen genannt, können ebenfalls Erreger aufnehmen und abbauen.
Phagozyten und Phagozytose
Phagozyten sind Immunzellen, die extrazelluläre Partikel, Mikroorganismen und Flüssigkeiten aufnehmen können und im Inneren der Zelle zersetzen. Dieser Vorgang wird Phagozytose genannt.
Dendritische Zellen
Dendritische Zellen (Abbildung 6) sind Antigen-präsentierende Zellen. Ein Antigen ist eine Substanz oder Struktur, die vom Immunsystem als fremd erkannt wird und eine Immunantwort auslöst (meist Bakterien, Viren oder Pilze). Dendritische Zellen befinden sich an den Grenzflächen des Körpers (z. B. Haut, Schleimhaut) und nehmen dort Erreger auf. Anschließend wandern sie in Lymphknoten, wo sie den T-Zellen die Antigene präsentieren und damit das adaptive (erworbene) Immunsystem aktivieren.
Ihre besondere Fähigkeit ist es, als Bindeglied zwischen angeborener und adaptiver Immunantwort zu fungieren. Sie erkennen Gefahren, nehmen Kontakt zu Erregern auf, analysieren deren Struktur und übermitteln die Information zielgerichtet an Lymphozyten.
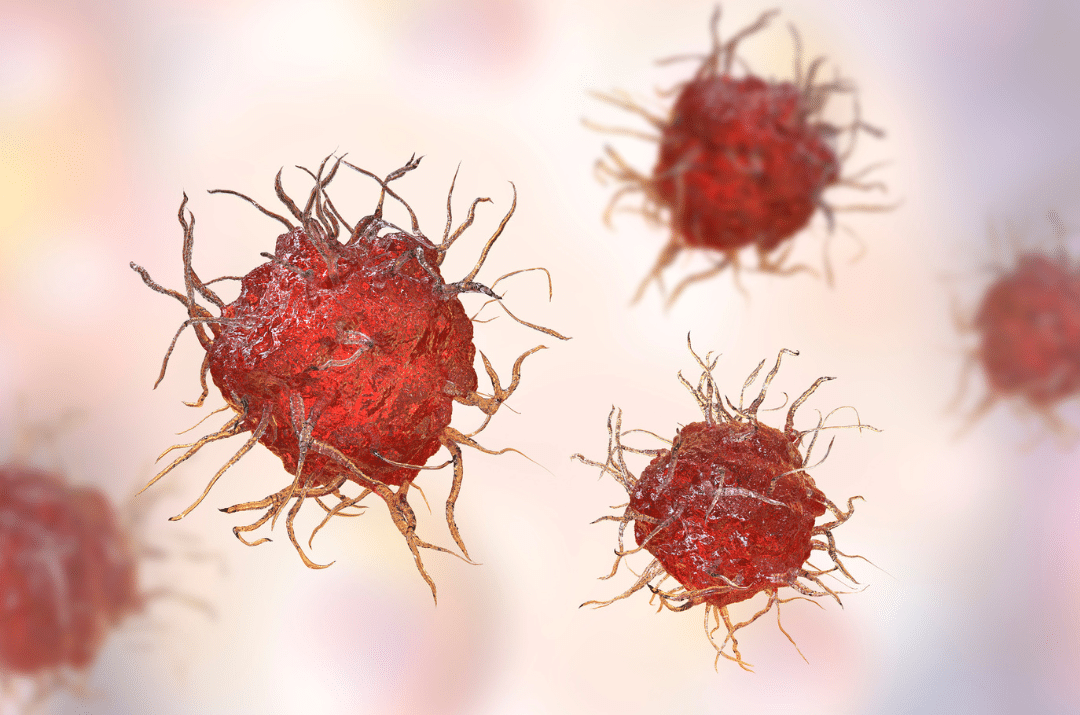
Abbildung 6 Dendritische Zellen sind das Bindeglied zwischen angeborener und erworbener Immunantwort.
Natürliche Killerzellen (NK-Zellen)
NK-Zellen (Abbildung 7) sind spezialisierte Lymphozyten des angeborenen Immunsystems. Sie erkennen virusinfizierte Zellen und tumorartige Zellen. Sie erkennen insbesondere auch solche Zellen, die ihre MHC-I-Moleküle herunterregulieren, was ein typischer „Trick“ von Viren zur Immunflucht ist.
NK-Zellen töten solche Zellen durch Freisetzung von Perforin und Granzym. Das sind Botenstoffe, die sie im Inneren in Bläschen gespeichert habe. Sie wirken zytotoxisch und lösen so den programmierten Zelltod (Apoptose) aus. Zusätzlich setzen sie Interferon-gamma (IFN-γ) frei, das Makrophagen aktiviert und die antivirale Abwehr verstärkt.
Abbildung 7 Natürliche Killerzellen (NK-Zellen) kümmern sich u.a. um die Virenabwehr.
Mastzellen und basophile Granulozyten
Mastzellen befinden sich hauptsächlich in Geweben und Schleimhäuten, insbesondere in der Nähe von Blutgefäßen und Nerven. Sie enthalten Granula mit Histamin, Heparin und anderen Mediatoren, die bei Aktivierung freigesetzt werden. Mastzellen spielen eine zentrale Rolle bei allergischen Reaktionen und sind auch wichtig bei der Abwehr von Parasiten.
Einen kleinen Überblick über einige Mastzellbotenstoffe und deren gesundheitlichen Auswirkungen erfährst du hier: “Mastzellaktivierung – Histamin ist nicht alles“
Basophile Granulozyten sind funktionell ähnlich, zirkulieren aber hauptsächlich im Blut. Beide Zelltypen fördern Vasodilatation (Erweiterung der Blutgefäße), erhöhte Gefäßpermeabilität und Leukozytenmigration, was die Einleitung einer lokalen Entzündung erleichtert.

Abbildung 8 Mastzellen sind die Hauptakteure bei allergischer Entzündung.
Eosinophile Granulozyten
Eosinophile sind spezialisiert auf die Abwehr von Parasiten (Abbildung 9), insbesondere Helminthen (Würmer). Sie enthalten zytotoxische Enzyme, darunter Major Basic Protein (MBP) und Peroxidase. Diese Botenstoffe können auf größere Parasiten wirken, die nicht phagozytiert werden können.
Zudem sind sie an allergischen Reaktionen beteiligt und werden bei chronischen Entzündungsprozessen, z. B. bei Asthma bronchiale oder eosinophiler Ösophagitis, vermehrt gefunden.
Abbildung 9 Eosinophile können nicht nur in allergische Prozesse involviert sein, sondern auch in der Bekämpfung von Parasiten.
Zusammenfassung
Die angeborene Immunabwehr ist unsere erste Verteidigungslinie. In diesem ersten Teil hast du erfahren, welche Barrieren und Zellen zu dieser Immunantwort gehören, die sofort auf Bedrohungen reagieren kann. Während Haut, Schleimhäute und chemische Schutzmechanismen verhindern, dass Krankheitserreger überhaupt eindringen, sorgen spezialisierte Immunzellen dafür, dass eingedrungene Mikroben erkannt und eliminiert werden. So bildet das angeborene System ein robustes Grundgerüst, das nicht nur Infektionen eindämmt, sondern auch den Weg für die gezielte Arbeit des adaptiven Immunsystems bereitet.
So geht es in Teil 2 weiter
Was ist das Komplementsystem und wie funktioniert es?
Welche Auswirkungen hat es auf die Aktivität von Immunzellen, wie Mastzellen?
Was bedeutet die Aktivierung des Komplementsystems für die körpereigene Histaminausschüttung?
Abonniere unseren Newsletter, wenn du nichts verpassen möchtest!
Du wirst als Erstes informiert, wenn wir neue Produkte haben, es neue Artikel im Science Blog gibt oder wenn eine Rabattaktion stattfindet.
Quellen
- Murphy, K.M., 2011. Janeway’s Immunobiology. London, UK: Taylor & Francis Group.
- Abbas, A.K., Lichtman, A.H., Pillai, S., 2022. Cellular and Molecular Immunology. 10th edition. Philadelphia, Pennsylvania: Elsevier.
- Medzhitov R, Janeway C Jr. Innate immune recognition: mechanisms and pathways. Immunol Rev. 2000 Feb;173:89-97. doi: 10.1034/j.1600-065x.2000.917309.x. PMID: 10719670.
- Iwasaki A, Medzhitov R. Control of adaptive immunity by the innate immune system. Nat Immunol. 2015 Apr;16(4):343-53. doi: 10.1038/ni.3123. PMID: 25789684; PMCID: PMC4507498.
- Mantovani A, Cassatella MA, Costantini C, Jaillon S. Neutrophils in the activation and regulation of innate and adaptive immunity. Nat Rev Immunol. 2011 Jul 25;11(8):519-31. doi: 10.1038/nri3024. PMID: 21785456.
- Ricklin D, Hajishengallis G, Yang K, Lambris JD. Complement: a key system for immune surveillance and homeostasis. Nat Immunol. 2010 Sep;11(9):785-97. doi: 10.1038/ni.1923. Epub 2010 Aug 19. PMID: 20720586; PMCID: PMC2924908.
- Suttorp, N., Döring, A., Beer, M., 2016. Harrison’s Innere Medizin. 19. Auflage. Berlin: ABW Wissenschaftsverlag.
- Sattler, S., 2017. The role of the immune system beyond the fight against infection. Advances in Experimental Medicine and Biology, 1003, pp.3–14. DOI: 10.1007/978-3-319-57613-8_1.
- Houssaint, E., Sai, P., 1988. Le développement du système immunitaire [Development of the immune system]. Annales d’Endocrinologie (Paris), 49(1), pp.68–76. [French]. PMID: 3261570.
- Margulies, D., 2000. Induction of immune responses. Current Protocols in Immunology, 89. Available at: https://doi.org/10.1002/0471142735.im0200s89.
- Paul, W.E., 1993. Fundamental Immunology. 3rd edition. New York: Raven Press.
Sie sehen gerade einen Platzhalterinhalt von Vimeo. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr InformationenSie sehen gerade einen Platzhalterinhalt von YouTube. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr InformationenSie sehen gerade einen Platzhalterinhalt von Facebook. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr InformationenSie sehen gerade einen Platzhalterinhalt von Instagram. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr InformationenSie sehen gerade einen Platzhalterinhalt von TrustIndex. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr InformationenSie sehen gerade einen Platzhalterinhalt von X. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr Informationen
