
Histamin – unser Freund und Feind
Inhaltsverzeichnis
Wenn man die Datenbank PubMed des National Center for Biotechnology Information (NCBI) nach dem Schlagwort Histamin (Siehe Abbildung 1) durchsucht, liefert die Suche 90.001 Ergebnisse (Stand: Januar 2021). Um die Recherche für den Artikel nicht Jahre in Anspruch nehmen zu lassen, habe ich die Suche nur auf Reviews – also Übersichtsartikel – eingegrenzt, um einen aktuellen Überblick über das Thema geben zu können. Das half aber auch nur bedingt weiter. Man erhält trotzdem noch 9.496 Ergebnisse. Histamin hat also schon sehr intensiv die Aufmerksamkeit der Forscher auf sich gezogen, was die Vermutung nahelegt, dass es ein sehr wichtiger Bestandteil der menschlichen Physiologie sein muss – und ja das ist es.
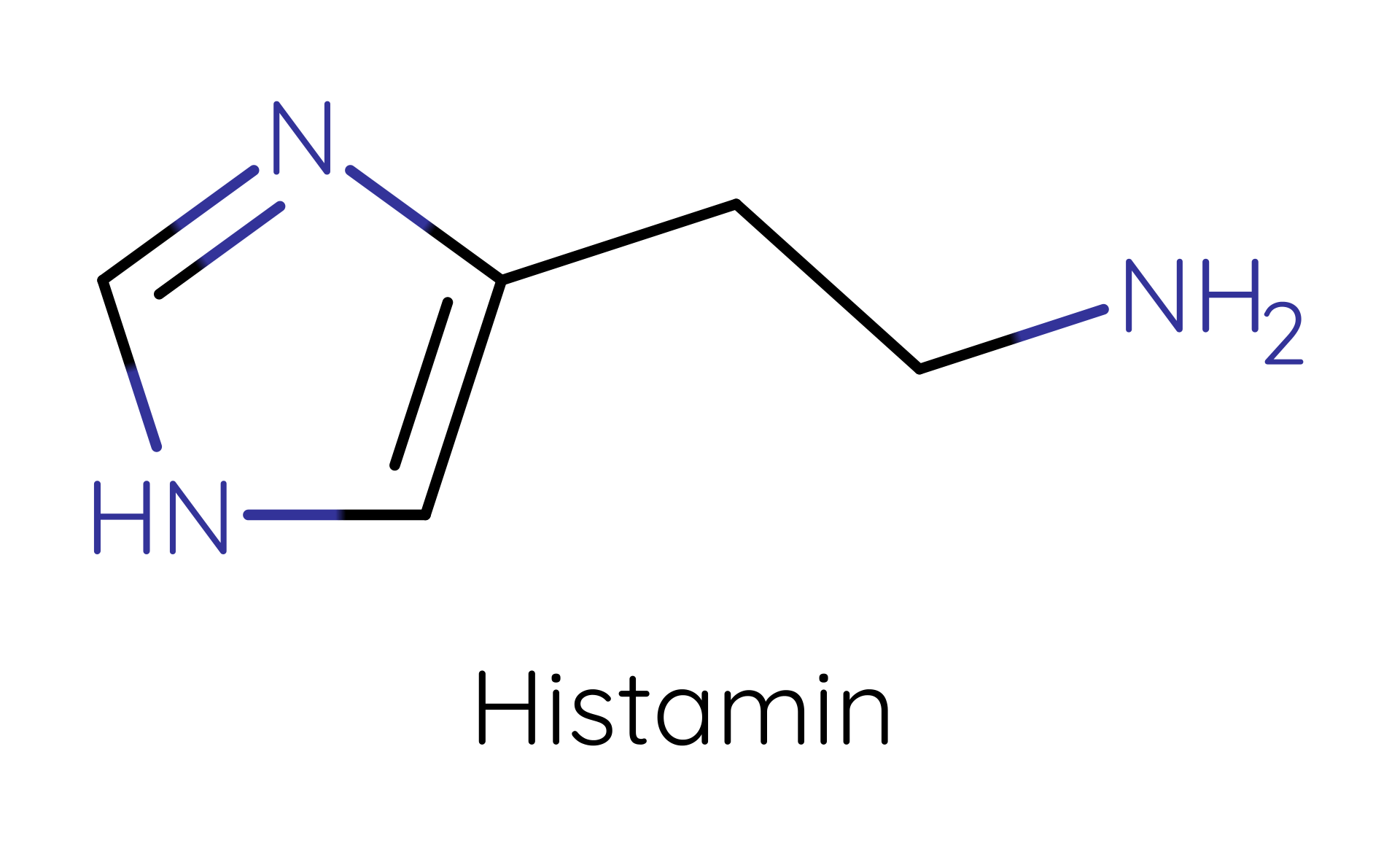
Abbildung 1 Histamin oder auch „2-(4-Imidazolyl)-ethylamin“. Abgeleitet wird der Name vom griechischen ιστός ‚histos‘, dem Wort für Gewebe.
Synthetisiert wurde es 1907 zum ersten Mal mehr oder weniger zufällig von den beiden Chemikern, A. Windaus und W. Vogt.1 So wie es aussieht hatten sie aber noch keinen blassen Schimmer, was für eine vielseitige Substanz sie da erzeugt hatten. Sie schrieben “Wir haben diese eigenartige Substanz noch nicht genauer untersucht”.
In den letzten knapp 115 Jahren hat sich anschließend einiges getan und man weiß mittlerweile schon eine ganze Menge über diese „eigenartige Substanz“. Es gehört zu den meistuntersuchten physiologisch wirksamen Molekülen.
Als richtiger Tausendsassa hat es sowohl physiologische, also für jeden gesunden Menschen wichtige, als auch pathophysiologische, also krankhaft verändernde Wirkungen.
1. Substanzklasse von Histamin
Histamin ist ein Gewebshormon und gehört zu den biogenen Aminen, die hauptsächlich durch die enzymatische Decarboxylierung von Aminosäuren entstehen. Dazu gehören z.B. auch Tyramin, welches aus der Aminosäure Tyrosin gebildet wird und auch Serotonin, das aus 5-Hydroxytryptophan gebildet wird. Sie werden sowohl von Lebewesen als auch Pflanzen gebildet und sind somit ein allgegenwärtiger Bestandteil des Lebens.2
2. Vorkommen
Histamin wird im Körper vor allem in Mastzellen und Basophilen3,4, aber auch in enterochromaffinen Zellen im Magen, in Lymphknoten, dem Thymus und in histaminergen Neuronen gespeichert.3–7 Es gibt aber auch eine Reihe anderer Immun- und Nicht-Immunzellen und Gewebearten, die unter physiologischen und pathologischen Bedingungen Histamin enthalten.8 Die Zellen speichern das Histamin in zytoplasmatischen Granula – man kann sie sich als kleine Tröpfchen innerhalb der Zellen vorstellen – die nach Aktivierung der Zellen mit der Zellmembran verschmelzen und die enthaltenen Botenstoffe nach außen abgeben. Diesen Vorgang nennt man Degranulation.3
Darüber hinaus kommt Histamin in unterschiedlichen Lebensmitteln vor und wird auch von Mikroorganismen gebildet, die teilweise auch zur Herstellung von Lebensmitteln verwendet werden (z.B. Joghurt, Sauerkraut). Doch dazu an andere Stelle mehr.
3. Wirkungsmechanismus
Histamin ist ein Molekül, welches über die Aktivierung von vier Rezeptoren – H1, H2, H3 und H4 – seine Wirkung im menschlichen Körper entfalten kann. Die vier Rezeptoren unterscheiden sich in ihrer Affinität zu Histamin, also der Stärke mit welcher Histamin an sie binden kann. H1 und H2 Rezeptoren haben eine niedrige Affinität, während H3 und H4 Rezeptoren eine hohe Affinität zu Histamin besitzen (Abbildung 2).8
Auch die Wirkung der Rezeptoren ist unterschiedlich. H1 Rezeptoren haben z.B. einen inotropen Effekt auf das Herz. Dadurch wird die Schlagkraft erhöht. Auf der anderen Seite haben H2 Rezeptoren einen chronotropen Effekt auf das Herz, wodurch die Schlagfrequenz des Herzens steigt.9 Diesen Effekt kennen viele Menschen mit einer Histamin-Metabolisierungsstörung nur zu gut. Das könnte auch erklären, warum kardiale Symptome wie der erhöhte Puls oft besser auf H2-Antihistaminika ansprechen.
Die H1-4 Rezeptoren gehören zu den sog. GPCRs, den G-Protein gekoppelten Rezeptoren. Viele von diesen haben die Möglichkeit auch ohne Agonist aktiv zu sein, also eine gewisse dauerhafte Grundaktivität zu zeigen, die durch Agonisten und Antagonisten verstärkt oder abgeschwächt werden kann. Dies ist für H1-3 der Fall.9
4. Physiologische Eigenschaften
Histamin trägt zur Regulation der Physiologie bei, indem es auf die Magensaft-Sekretion, Neurotransmission und Immunantwort Einfluss nimmt (Abbildung 2).8 Außerdem ist es an der Kontraktion glatter Muskelzellen, der Vasodilatation und Zytokinproduktion beteiligt.7 Gezeigt werden konnte auch, dass histaminerge Neuronen Projektionen in alle möglichen Bereiche des Gehirns besitzen und es so an vielfältigen Prozessen wie z.B. Wachsamkeit, Schlaf/Schlaflosigkeit, Nahrungsaufnahme, sowie an endokrinen Abläufen und Gedächtnisprozessen beteiligt ist.10 Es hat aber auch pathophysiologisches Potential, welches vor allem im Zusammenhang mit allergisch-entzündlichen Erkrankungen und Schlaflosigkeit bekannt geworden ist.8,11
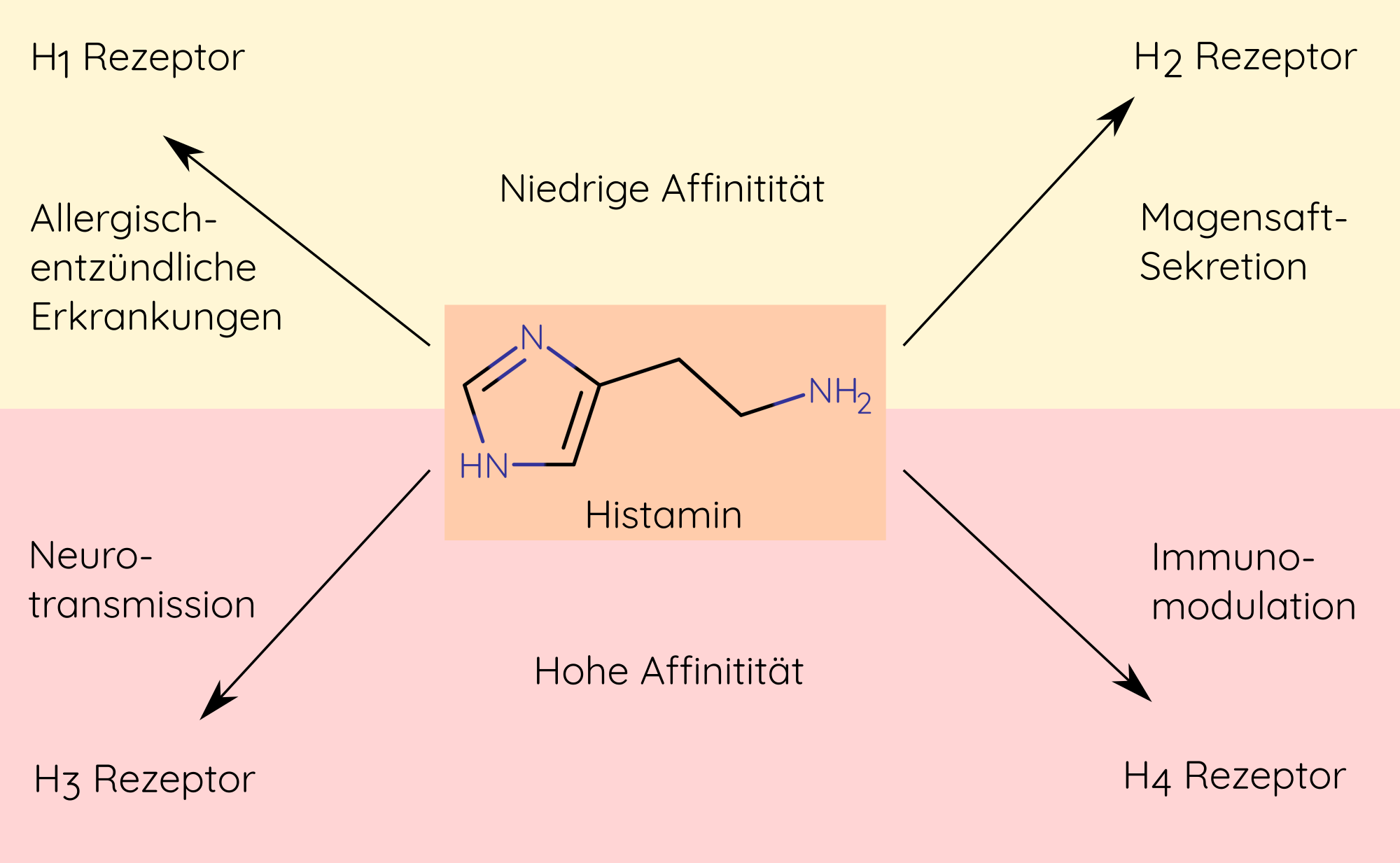
Abbildung 2 Histaminrezeptoren und deren Funktion.
5. Pathophysiologische Eigenschaften – Auswirkungen eines zu hohen Histamingehalts im Blut
Es konnte gezeigt werden, dass gesunde Menschen, denen 0,25 mg – 0,5 mg Histaminphosphat intravenös gespritzt wurde, folgende Symptome entwickelten12:
- Heftige, pulsierende Kopfschmerzen, mit einem Druckgefühl
- Flush im Gesicht (Rötung durch Weitstellung der kleine Blutgefäße)
- Leichte Veränderungen im Blutdruck, die von Person zu Person unterschiedlich ausfällt
- Anstieg des Liquor-Drucks (Gehirn-Rückenmarks-Flüssigkeit)
- Pulsanstieg um 10 – 20 Schläge pro Minute
- Ängstlichkeit
- Übelkeit und Erbrechen
- Durchfall
- Schwitzen
Bei subkutaner oder intramuskulärer Injektion höherer Dosen wurden noch andere Symptome beobachtet12:
- Generalisierte Vasodilatation (Weitstellung der Blutgefäße)
- Erhöhung der kutanen Temperatur
- Steiler Abfall des Blutdrucks
- Heftige Kopfschmerzen
- Sehstörungen
- Bronchospasmen und Atemnot
- Metallischer Geschmack
- Erbrechen
- Durchfall
- Vermehrte Speichel-, Magensaft- und Pankreassekretion
- Schock bei sehr schweren Fällen
Alle Menschen mit Allergien oder histaminvermittelten Unverträglichkeiten (z.B. Histaminintoleranz oder Salicylatintoleranz) kennen diese Symptome, wenn auch eher selten in der vollen wie oben beschriebenen Ausprägung. Sie sind mehr ein ständiger Begleiter, der einem ununterbrochen mal stärker mal leichter auf den Kopf schlägt, einem in den Magen boxt, das Atmen erschwert oder die Haut zum Jucken bringt, was den Alltag deutlich erschweren kann.
Sowohl die Histamin- als auch die Salicylatintoleranz gehören zu den sog. Pseudoallergien, bei denen es zu einem Ungleichgewicht zwischen Histaminbildung/-ausschüttung und dessen Abbau bzw. zu stärkerem Ansprechen auf ausgeschüttetes Histamin kommt als es bei einem gesunden Menschen der Fall wäre. Hier haben auch die Mastzellen ihre Finger im Spiel, weil sie durch Histamin direkt aktiviert werden können. Doch dazu mehr an anderer Stelle.
6. Stoffwechsel
Man konnte nachweisen, dass es in vielen Gewebesorten von Säugetieren in unterschiedlicher Konzentration vorkommt13 und in menschlichen Zellen vom Enzym Histidin Decarboxylase aus der semi-essenziellen Aminosäure L-Histidin gebildet wird14. Dieser Schritt ist abhängig von Pyridoxal-5‘-Phosphat (aktive Form des Vitamin B6).15
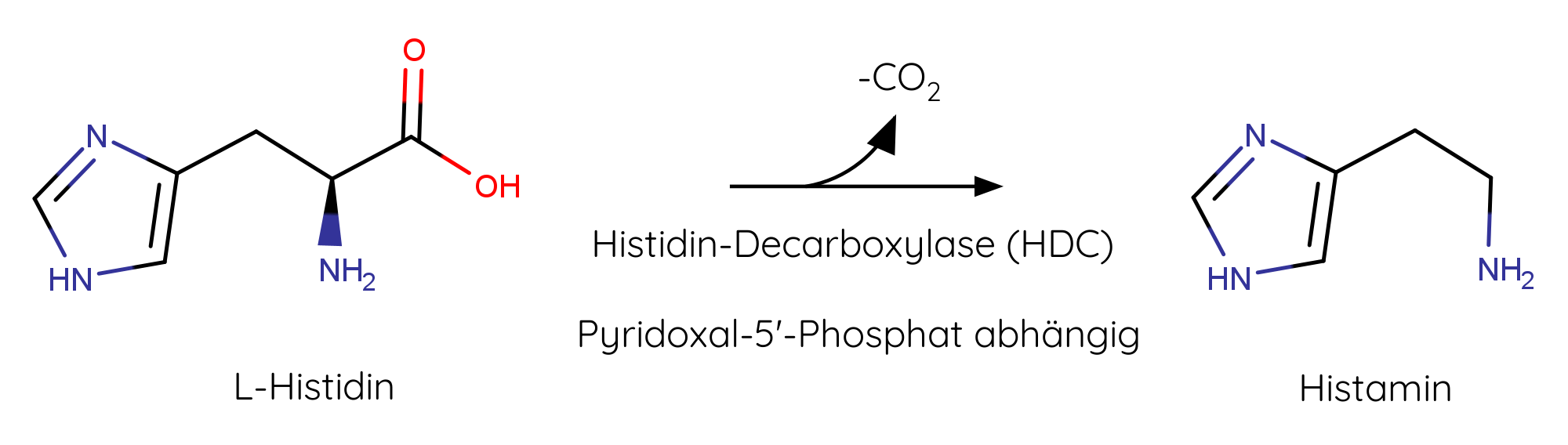
Abbildung 3 Pyridoxal-5‘-Phosphat abhängige Umwandlung von L-Histidin zu Histamin durch das Enzym Histidin-Decarboxylase (HDC).
Abgebaut wird es hauptsächlich von dem Kupfer-abhängigen Enzym Diaminoxidase (DAO) und in geringerem Ausmaß auch von dem Enzym Histamin-N-Methyltransferase (HNMT), welches als Cofactor S-Adenosylmethionin benötigt.16,17 Bei gesunden Menschen mit intakter Darmschleimhaut werden 99 % des aufgenommenen Histamins durch die DAO und davon weitere 80 % in der Leber durch die HNMT abgebaut, wodurch der größte Teil des Histamins nicht in den Blutkreislauf gelangt.18,19
Während die DAO vor allem in Vesikeln im Cytoplasma der Mikrovilli der Darmschleimhaut vorkommt20,21, von wo aus sie in den Darm abgegeben wird22, wird die HNMT in vielen Gewebearten gebildet und liegt frei im Cytosol vor. Vor allem in Nieren und Leber, aber auch in Milz, Dickdarm, Prostata, Eierstöcken, Rückenmarkszellen, Luftröhre und Lunge.23,24 Beim Abbau der Zwischenprodukte, die durch DAO und HNMT entstehen, ist auch die Aldehyddehydrogenase beteiligt.7 Diese wird auch benötigt, um Ethanol abzubauen. Gleichzeitig hat Alkohol noch zwei weitere Effekte. Er hemmt die DAO und kann dazu führen, dass Mastzellen degranulieren.23 So kann Alkohol Histamin-bedingte Symptome verstärken.
7. Zusammenfassung
Auch wenn Histamin oft als Übeltäter dargestellt wird, so ist es trotzdem ein vielseitig physiologisch aktives Hormon mit sehr wichtigen Aufgaben. Die Ursache, dass es in negatives Licht geraten ist, ist der Zusammenhang, der zwischen Histaminausschüttung und Symptomen bei Allergien und Pseudoallergien hergestellt werden konnte.
Du wirst als Erstes informiert, wenn wir neue Produkte haben, es neue Artikel im Science Blog gibt oder wenn eine Rabattaktion stattfindet.
Quellen
- Windaus A, Vogt W. Synthese des Imidazolyl-äthylamins. Ber Dtsch Chem Ges. 1907;40(3):3691-3695. doi:10.1002/cber.190704003164
- Santos MHS. Biogenic amines: their importance in foods. International Journal of Food Microbiology. 1996;29(2-3):213-231. doi:10.1016/0168-1605(95)00032-1
- Borriello F, Iannone R, Marone G. Histamine Release from Mast Cells and Basophils. In: Hattori Y, Seifert R, eds. Histamine and Histamine Receptors in Health and Disease. Vol 241. Handbook of Experimental Pharmacology. Springer International Publishing; 2017:121-139. doi:10.1007/164_2017_18
- GRAHAM HT, LOWRY OH, WHEELWRIGHT F, LENZ MA, PARISH HH JR. Distribution of Histamine among Leukocytes and Platelets. Blood. 1955;10(5):467-481. doi:10.1182/blood.V10.5.467.467
- Rubin W, Schwartz B. Electron microscopic radioautographic identification of the ECL cell as the histamine-synthesizing endocrine cell in the rat stomach. Gastroenterology. 1979;77(3):458-467. doi:10.1016/0016-5085(79)90005-2
- Riley JF, West GB. The presence of histamine in tissue mast cells. J Physiol. 1953;120(4):528-537. doi:10.1113/jphysiol.1953.sp004915
- Comas-Basté O, Sánchez-Pérez S, Veciana-Nogués MT, Latorre-Moratalla M, Vidal-Carou M del C. Histamine Intolerance: The Current State of the Art. Biomolecules. 2020;10(8). doi:10.3390/biom10081181
- Tiligada E, Ennis M. Histamine pharmacology: from Sir Henry Dale to the 21st century: Histamine pharmacology. British Journal of Pharmacology. Published online December 2, 2018. doi:10.1111/bph.14524
- Parsons ME, Ganellin CR. Histamine and its receptors. Br J Pharmacol. 2006;147 Suppl 1:S127-135. doi:10.1038/sj.bjp.0706440
- Haas H, Panula P. The role of histamine and the tuberomamillary nucleus in the nervous system. Nat Rev Neurosci. 2003;4(2):121-130. doi:10.1038/nrn1034
- Monnier M, Fallert M, Bhattacharya IC. The waking action of histamine. Experientia. 1967;23(1):21-22. doi:10.1007/BF02142244
- Naranjo P. Toxicity of Histamine: Lethal Doses. In: Rocha e Silva M, ed. Histamine and Anti-Histaminics. Springer Berlin Heidelberg; 1966:179-201. doi:10.1007/978-3-662-12016-3_9
- Cohn H. A. SHORE, ALAN BURKHALTER. 1959;17:5.
- Huang H, Li Y, Liang J, Finkelman FD. Molecular Regulation of Histamine Synthesis. Front Immunol. 2018;9:1392. doi:10.3389/fimmu.2018.01392
- Mehta PK, Christen P. The molecular evolution of pyridoxal-5’-phosphate-dependent enzymes. Adv Enzymol Relat Areas Mol Biol. 2000;74:129-184. doi:10.1002/9780470123201.ch4
- Finney J, Moon H-J, Ronnebaum T, Lantz M, Mure M. Human copper-dependent amine oxidases. Archives of Biochemistry and Biophysics. 2014;546:19-32. doi:10.1016/j.abb.2013.12.022
- Martner-Hewes PM, Hunt IF, Murphy NJ, Swendseid ME, Settlage RH. Vitamin B-6 nutriture and plasma diamine oxidase activity in pregnant Hispanic teenagers. The American Journal of Clinical Nutrition. 1986;44(6):907-913. doi:10.1093/ajcn/44.6.907
- Maslinski C, Fogel WA. Catabolism of Histamine. In: Uvnäs B, ed. Histamine and Histamine Antagonists. Vol 97. Handbook of Experimental Pharmacology. Springer Berlin Heidelberg; 1991:165-189. doi:10.1007/978-3-642-75840-9_14
- Schwelberger HG, Weidenhiller M, Hahn EG, Raithel M, Kuefner MA. Both catabolic pathways of histamine via histamine-N-methyltransferase and diamine oxidase are diminished in the colonic mucosa of patients with food allergy. Inflammation Research. 2004;53(0):S31-S32. doi:10.1007/s00011-003-0314-5
- Bieganski T, Kusche J, Lorenz W, Hesterberg R, Stahlknecht C, Feussner K. Distribution and properties of human intestinal diamine oxidase and its relevance for the histamine catabolism. Biochimica et Biophysica Acta (BBA) – General Subjects. 1983;756(2):196-203. doi:10.1016/0304-4165(83)90092-2
- Schwelberger HG. Analysis of tissue and subcellular localization of mammalian diamine oxidase by confocal laser scanning fluorescence microscopy. Inflammation Research. 1998;47(0):60-61. doi:10.1007/s000110050273
- Daniele B, Quaroni A. Polarized secretion of diamine oxidase by intestinal epithelial cells and its stimulation by heparin. Gastroenterology. 1990;99(6):1675-1687. doi:10.1016/0016-5085(90)90474-F
- Maintz L, Novak N. Histamine and histamine intolerance. Am J Clin Nutr. 2007;85(5):1185-1196. doi:10.1093/ajcn/85.5.1185
- Kovacova-Hanuskova E, Buday T, Gavliakova S, Plevkova J. Histamine, histamine intoxication and intolerance. Allergologia et Immunopathologia. 2015;43(5):498-506. doi:10.1016/j.aller.2015.05.001
Kommentare
Füge einen Kommentar hinzu
Du musst angemeldet sein, um einen Kommentar abzugeben.
Sie sehen gerade einen Platzhalterinhalt von Vimeo. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr InformationenSie sehen gerade einen Platzhalterinhalt von YouTube. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr InformationenSie sehen gerade einen Platzhalterinhalt von Facebook. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr InformationenSie sehen gerade einen Platzhalterinhalt von Instagram. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr InformationenSie sehen gerade einen Platzhalterinhalt von TrustIndex. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr InformationenSie sehen gerade einen Platzhalterinhalt von X. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr Informationen

Hallo Thomas,
ich habe eine Histamin-,/Laktose-/Fruktose-, Salicylatunverträglichkeit und noch diverse Allergien (Sulfit, Nickel etc.) und der Leidensdruck ist seit 1 Jahr leider recht groß. Außerdem finde ich es sehr sehr schwierig, geeignete Medikamente/Nahrungsergänzungsmittel/
Kosmetika etc. ohne Farb-/Duft- und Konservierungsstoffe sowie ohne pflanzliche Zusätze und ätherische Öle zu finden und daher bin ich sehr gespannt auf deinen neuen Blog und auf neue interessante Artikel, die mir vielleicht etwas mehr Aufschluss über die ganzen Zusammenhänge geben und somit die Möglichkeit, meine Unverträglichkeiten besser und lebenswerter in den Griff zu bekommen. Liebe Grüße BiFa
Hallo BiFa,
da kann ich dich voll und ganz verstehen. Mir ging es genauso. Es ist schwierig verträgliche Nahrungsergänzungsmittel und Körperpflegeprodukte zu finden, wenn man mehrere Baustellen hat. Dieses Problem möchten wir mit unseren Produkten lösen und wir wissen aus eigener Erfahrung, dass das Wissen über die Zusammenhänge unglaublich hiflreich ist, um solche Erkrankungen besser managen zu können.
Liebe Grüße
Thomas